Keskeinen ero: elektronegatiivisuus on kemiallinen ominaisuus, joka päättää atomin taipumuksesta houkutella elektroneja kovalenttisessa sidoksessa. Se on ominaisuus, jota ei voida mitata suoraan. Atomin elektronin affiniteetti on energiamäärä, jonka atomi saa aikaan, kun elektroni lisätään neutraaliin atomiin tai molekyyliin, jotta se saadaan negatiiviseksi ioniksi. Kiinteän olomuodon fysiikassa tunnetaan myös elektronien affiniteettia energiana, joka tarvitaan elektronin siirtämiseksi alimman johtosarjan pohjasta kiinteään tilaan läheisessä tyhjiössä.

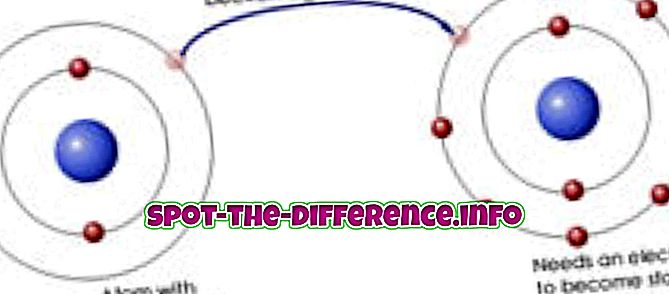
Elektronegatiivisuus on kemiallinen ominaisuus, joka päättää atomin taipumuksesta houkutella elektroneja kovalenttisessa sidoksessa. Se on ominaisuus, jota ei voida suoraan mitata ja johon atomin atomiluku ja etäisyys, jonka sen valenssielektronit sijaitsevat ladatusta ytimestä, vaikuttavat. Näin ollen mitä korkeampi yhdisteen tai elementin elektronegatiivisuus, sitä enemmän se houkuttelee elektroneja kohti sitä. Elektronegatiivisuuden käsitettä ehdotti Linus Pauling vuonna 1932 valenssisideteorian lisänä. Koska elektronegativiteettia ei voida suoraan mitata, se lasketaan atomin atomi- ja molekyyliominaisuuksilla, kuten ydinvaraus, ja muiden atomien kuorissa olevien elektronien lukumäärä / sijainti.

Vaikka ne ovat keskenään samanlaisia ja mittaavat atomin taipumusta houkutella elektroneja; niillä on vain vähän eroja. Eräs merkittävä ero on se, että elektronegatiivisuuden käsite ei ole mitattavissa ja sitä käytetään ensisijaisesti selittämään kovalenttisia sidoksia ja sidospolariteettia. Elektronin affiniteetti on kuitenkin kvantifioitavissa ja se voidaan helposti mitata mittaamalla vapautuneen energian määrä, kun elektroni lisätään. Elektronegatiivisuus auttaa myös ymmärtämään elektronien parin sijainnin. Elektronegatiivisuus käsittelee yksittäisiä atomeja, kun taas elektronin affiniteetti käsittelee molekyylin atomeja. Elektronegatiivisuus on myös ominaisuus, kun taas elektronin affiniteetti on mittaus. Elektronegatiivisuusarvot voivat myös muuttua riippuen molekyylistä, jota se sitoo, kun taas elektronin affiniteetti ei muutu.