Keskeinen ero: Ioninen sidos on kahden erilaisen (eli metalli- ja ei-metallisen) atomin välinen kemiallinen sidos, jossa yksi atomi luopuu elektronista toiselle. Kovalenttinen sidos on toinen vahva kemiallinen sidos. Se on ollut samanlainen atomi (eli kaksi ei-metallia). Kovalenttisessa sidoksessa nämä kaksi atomia kokoontuvat jakamaan elektronin sen sijaan, että atomi ottaa elektronin toisesta.
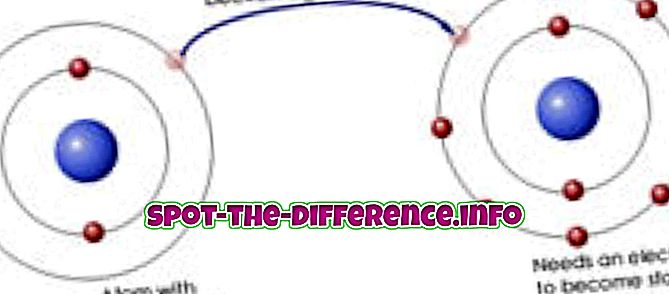
Ioninen sidos on kemiallinen sidos kahden erilaisen (eli metalli- ja ei-metallisen) atomin välillä, jossa yksi atomi luopuu elektronista toiselle. Näin ollen molemmat atomit tulevat ioneiksi, koska yhdellä atomilla on yksi elektroni vähemmän, kun taas toisessa on ylimääräinen. Elektronin menettäneellä metalli-ionilla on positiivinen varaus. Elektronin saaneella ei-metallisella ionilla on negatiivinen varaus. Kun vastakohdat houkuttelevat, nämä ionit houkuttelevat sitten voimakkaasti toisiaan niin voimakkaasti, että ne tulevat sitoutumaan.
Ioniset yhdisteet ovat tavallisesti kiintoaineita, eli suoloja. Ne ovat hyvin liukoisia veteen ja niillä on korkea sulamispiste. Kun ne ovat vedessä, niillä on myös suuri sähköjohtavuus.

Kovalenttinen sidonta sisältää monenlaisia vuorovaikutuksia, mukaan lukien σ-sidonta, π-sidonta, metalli-metalli-sitoutuminen, agostinen vuorovaikutus ja kolmikeskinen kaksielektroninen sidos. Kun atomissa on elektroni sen ulkokuoressa ja toinen atomi vaatii elektronin täyttämään sen ulkokuoren, molemmat atomit yhdessä yhdessä jakamaan elektronin. Näin ollen molemmilla atomeilla on täydellinen ulompi kuori ja vastaavasti stabiili elektroninen konfiguraatio.
Kemialliset sidokset tehdään siten, että atomilla voi olla täysi ulompi kuori, sillä täysi ulompi kuori tarkoittaa stabiilia elektronista konfiguraatiota. Ionisessa sidoksessa, kun metalliatomilla on yksi elektroni ulommassa kuoressaan ja ei-metalli tarvitsee elektronin täyttääkseen sen ulkokuoren, metalliatomi antaa elektroninsa ei-metallille. Vastaavasti kovalenttisessa sidoksessa ne jakavat elektronin yhtä hyvin.
Ionisidos | Kovalenttisidos | |
Määritelmä | Kemiallinen sidos kahden erilaisen atomin välillä, joissa atomi luopuu elektronista toiselle. | Kovalenttinen sidos on kemiallinen sidos, joka sisältää elektronien jakamisen kahden samanlaisen atomin välillä. |
esiintyminen | Metalli ja ei-metalli | Kaksi ei-metallia |
Vastakkaisuus | Korkea | Matala |
Molekyylin muoto | Ei tarkkaa muotoa, ristikkorakenteita | Määritelty muoto |
Sähkönjohtavuus | Korkea | Yleensä ei mitään |
Lämmönjohtokyky | Korkea | Yleensä alhainen |
Aineen sulamispiste | Vaihtelee, mutta yleensä korkeampi kuin kovalenttiset yhdisteet | Vaihtelee, mutta yleensä pienempi kuin ioniset yhdisteet |
Aineen kiehumispiste | Korkea | Vaihtelee, mutta yleensä pienempi kuin ioniset yhdisteet |
Vesiliukoisuus | Korkea | Vaihtelee, mutta yleensä pienempi kuin ioniset yhdisteet |
Aineen tila huoneen lämpötilassa | Yleensä kiinteä | Kiinteä, nestemäinen, kaasu |