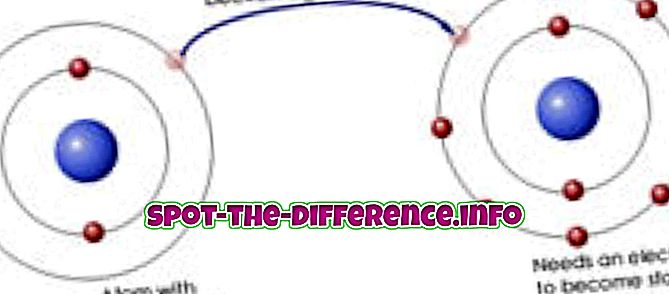
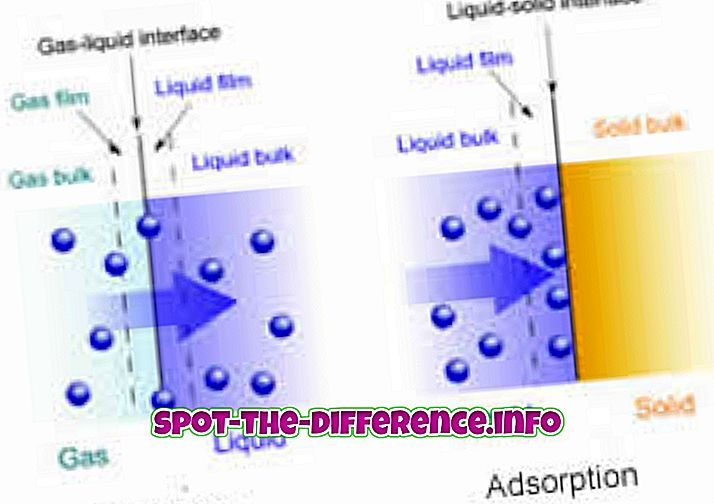
Keskeinen ero: Absorptio on suurin ilmiö, jossa absorbentti tunkeutuu täysin kiinteän tai nestemäisen aineen runkoon muodostaen yhdisteen tai liuoksen. Toisaalta adsorptio on pinnan ilmiö, jossa adsorbaatin molekyylit keskittyvät vain adsorbentin pinnalle.
Kemiallinen reaktio - kaliumhiilen liuoksella absorboitunut hiilidioksidi
Fyysinen prosessi - Ilma imeytyy veteen liuottamalla

Adsorptiotiloja on kahdenlaisia - kemiallisia ja fyysisiä. Kemiallisessa adsorptiossa molekyylit ja pinta liimataan heikoilla Vander Walls -voimilla. Toisaalta kemiallisessa adsorptiossa molekyylien ja pinnan välille muodostuu kemiallinen sidos.
Siksi pääasiallinen ero adsorption ja absorption välillä on, että imeytyminen on suurin ilmiö, joka tarkoittaa sitä, että se tapahtuu koko aineen rungossa, kun taas adsorptio pysyy pinnan ilmiönä. Adsorptio on aina eksoterminen, kun taas imeytyminen on endotermistä. Sorptio sisältää sekä imeytymis- että adsorptioprosessit.
Adsorptiota ja absorptiota vertaillaan:
adsorptio | imeytyminen | |
Defintion | Kaasun tai nestemäisen aineen kerääntyminen kiinteän tai nestemäisen aineen pinnalle | Aineen diffuusio nesteeseen tai kiinteään aineeseen liuoksen tai yhdisteen muodostamiseksi |
esimerkki | Inertti kaasut adsorboituvat puuhiilellä. | Kuiva sieni imee vettä |
Lämmönvaihto | Eksoterminen lukuun ottamatta H2: n adsorptiota lasiin | endoterminen |
Tasapainon saavuttaminen | Verrattain nopeammin | Verrattain hitaasti |
keskittyminen | Pitoisuus adsorbentin pinnalle on erilainen kuin irtotavarana | Konsentraatio pysyy samana koko materiaalissa |
Esiintymistiheys | Se on aluksi nopea, mutta myöhemmin sen nopeus alkaa laskea | Se tapahtuu yhtenäisellä hinnalla |