Keskeinen ero: Kemiallinen reaktio on prosessi, jossa elementin atomit järjestävät itsensä uudelleen muodostaakseen uuden aineen. Ydinreaktio on prosessi, jossa atomin ytimen rakenne muuttuu energian vapautumisen myötä.
Tärkein ero ydinreaktion ja kemiallisen reaktion välillä voidaan ymmärtää sen perusteella, miten reaktio tapahtuu atomissa. Ydinreaktio tapahtuu atomin ytimessä; atomin elektronit ovat vastuussa kemiallisista reaktioista.
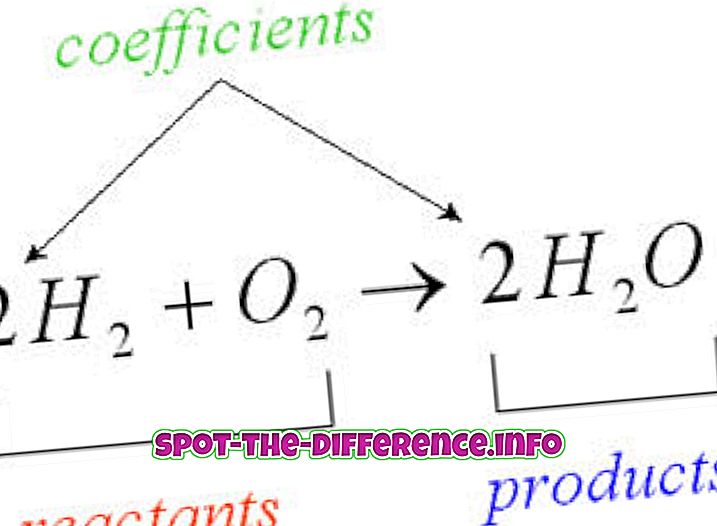
Yhtälöitä, kuten katalyyttejä, lämpötilaa, liuotinvaikutuksia, jne. Ohjaavat eri tekijät. Termodynaamisen tutkimuksen avulla reaktioita voidaan ohjata. Reaktionopeus yksinkertaisesti määrittää reaktion nopeuden. Se on parametri, joka tutkii, kuinka hidas tai nopea reaktio on. Esimerkiksi
Tarkastellaan seuraavaa reaktiota, jossa reagenssit A ja B menevät tuotteisiin C ja D.
a A + b B → c C + d D
Reaktion nopeus voidaan antaa joko kahdella reagoivalla aineella tai tuotteella.
Nopeus = -1 / a × d [A] / dt = -1 / b × d [B] / dt = 1 / c × d [C] / dt = 1 / d × d [D] / dt
Tässä a, b, c ja d ovat reagenssien ja tuotteiden kertoimia. Reagensseille on miinusmerkki, koska ne ovat tyhjentäviä
kun reaktio etenee. Koska tuotteet kasvavat, niille annetaan positiivisia merkkejä.

Ydinreaktiot käsittävät ytimen hajoamisen, koska se hajottaa atomin; se muodostaa uuden elementin protonien tai neutronien häviämisellä. Reaktio tapahtuu ytimen sisällä. Ydinreaktiossa on hyvin suuri energiamuutos. Se voidaan luokitella ydinfuusioon ja ydinfisioon. Fuusiossa kaksi tyyppistä ydintä yhdistetään vapauttamaan energiaa. Fissiossa suuri epävakaa ydin jaetaan kahteen pienempään stabiiliin tumaan ja energia vapautuu.
Kemiallisen ja ydinreaktion vertailu:
Kemiallinen reaktio | Ydinreaktio | |
Määritelmä | Elementit järjestävät itsensä uudelleen muodostaakseen uuden elementin. | Ytimen rakenne muuttuu energian vapauttamisen myötä. |
reaktio | Elektronit ovat vastuussa reaktiosta. | Se tapahtuu atomin ytimessä. |
asento | Se tapahtuu ytimen ulkopuolella. | Se tapahtuu ytimen sisällä. |
luonto | Sisältää elektronien häviämistä, vahvistumista ja jakamista. | Sisältää ytimen hajoamisen. |
energia | Alhainen energiamuutos. | Korkea energiamuutos. |
isotoopit | He reagoivat samoin | He reagoivat eri tavalla. |
Kemialliset yhdistelmät | Se on riippuvainen. | Se ei riipu. |
Massa | Reaktantit ja tuotteet ovat yhtä suuria. | Massa muuttuu. |